3D打印技術作為先進制造手段,在生物醫學領域掀起革新,尤其為微流控器件的一體化制備提供了核心技術支撐。對于罕見腫瘤病理切片的研究,樣本稀缺與多維分析需求的矛盾長期存在,而高精度3D打印能精準構建復雜的微通道、反應腔等關鍵微結構,以及快速一次成型自定義的PDMS芯片模具,縮短制樣周期并保證微通道與腔室的高重復性,為開發低樣本消耗、高集成度的病理分析設備奠定了基礎。針對病理切片與稀有腫瘤樣本的資源稀缺問題,將微流體模塊與高精度3D打印結合,能顯著降低所需切片數量并提升多通道和多標記的空間分辨率,使得組織切片處理、微量試劑流控與多通道并行檢測在臨床和研究中更加可及,成為破解臨床診斷與科研瓶頸的重要技術。
近日,海南大學的黃振立、史冰團隊在《Science Advances》在線發表題為“Dual-mode microfluidic immunostaining device for diagnostic biomarkers detection and tumor microenvironment evaluation”的原創性論著,海南大學的博士研究生張瑜為本文第一作者,海南大學的史冰講師和黃振立教授為共同通訊作者。該研究開發了雙模式微流控免疫染色裝置(Dumi),在1~2張組織切片上實現了免疫組織化學(IHC)標志物診斷流程與腫瘤微環境(TME)科研分析的一體化,并能構建含多個診斷標志物的空間TME圖譜,便于挖掘腫瘤細胞亞群與其原位微環境的關聯性。該文章為罕見腫瘤的精準診斷和TME研究提供了臨床可及的高效解決方案。
首先,研究團隊通過摩方精密的面投影微立體光刻(PμSL)3D打印技術(microArch? S240,精度:10 μm),制造了核心部件——3D打印流體交換歧管和微流控芯片模具,其微通道尺寸變異系數小于1%,確保了裝置的結構一致性與運行穩定性。Dumi裝置集成了雙模式染色功能:多通道模式通過16個平行微通道,可同時檢測16種診斷生物標志物;全腔室模式則能完成多輪循環迭代的免疫熒光染色,構建TME空間圖譜(圖1)。微流控系統的連續流動設計,將傳統1小時以上的孵育時間縮短至10分鐘,試劑消耗和切片使用量分別減少90%和94%以上,且可兼容常規顯微成像平臺。
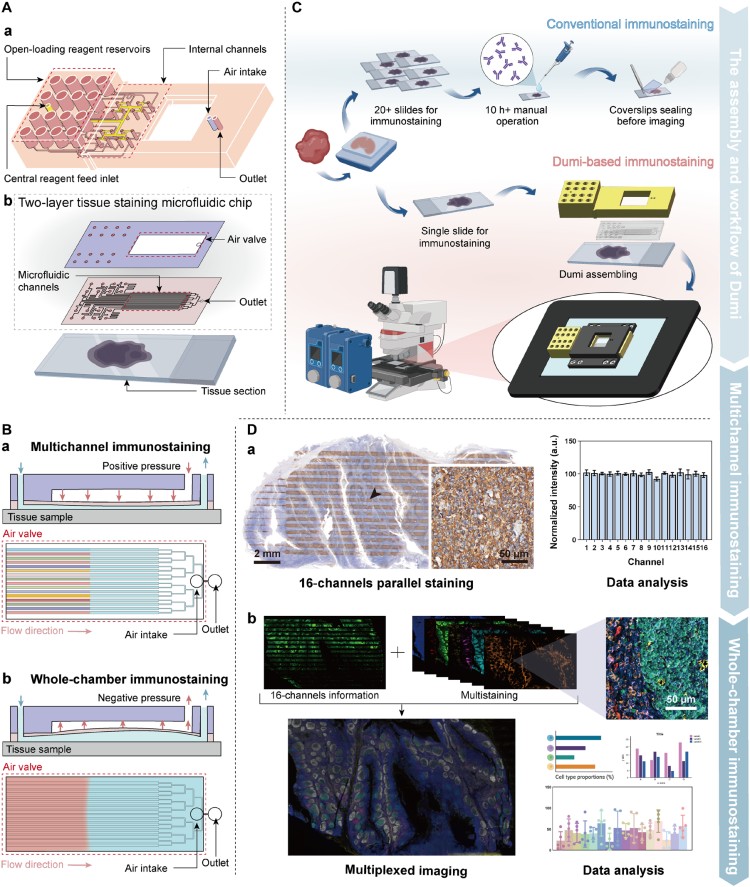
圖1. Dumi裝置結構、工作流程及雙染色模式示意圖。
為提升染色準確性,研究人員以CD20(膜標志物)和Ki67(核標志物)為對象,優化了流速和孵育時間(圖2)。結果顯示,4 μL/min流速、10分鐘孵育時,抗原-抗體結合接近飽和(CD20達92%、Ki67達84%),且非特異性背景最低。通過抗體濃度梯度實驗,驗證了在常規IHC推薦濃度下,Dumi可直接使用現有抗體,無需重新優化,兩種抗體的濃度-響應曲線形態相似,證明方法一致性較好。
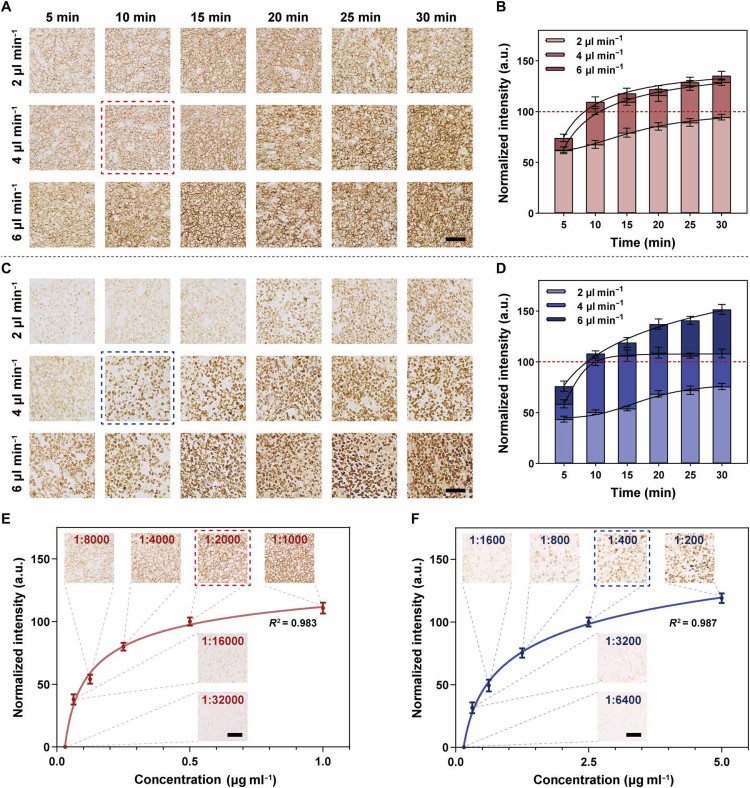
圖2. Dumi免疫染色參數優化。
接下來以扁桃體組織CD20染色為模型,對比Dumi全腔室模式與傳統IHC(圖3)。傳統IHC需235分鐘,且存在明顯邊緣效應;Dumi僅需34分鐘,且染色強度分布較為均勻。定量分析顯示,Dumi的信號變異系數(<9.307%)低于傳統方法(<11.450%),雖信號強度略低,但背景信號更低,信號背景比(SBR)更優,證明二者信號提取能力相當,可相互替代。
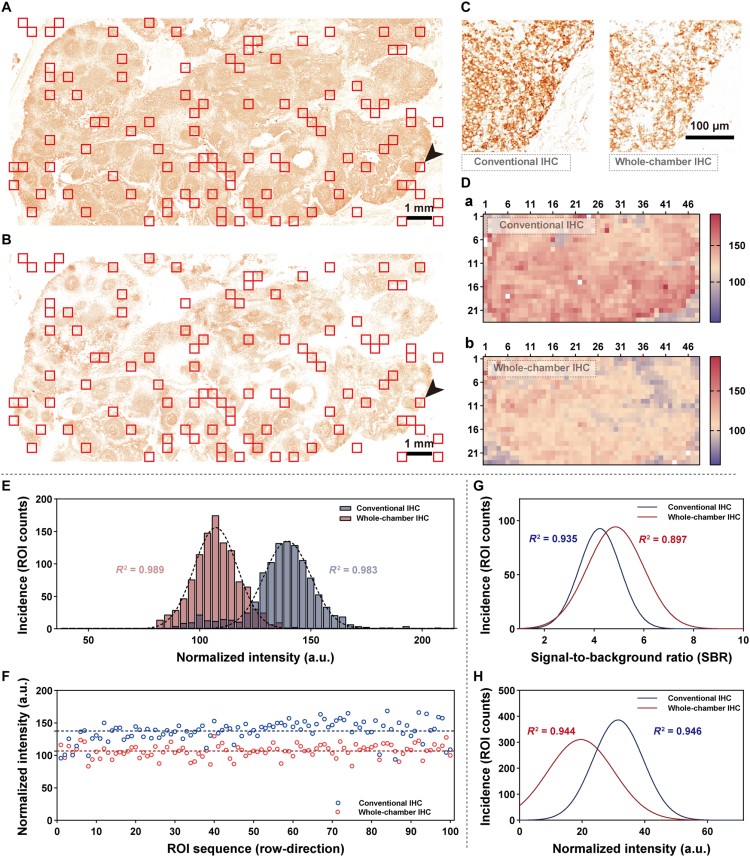
圖3. 全腔室模式與傳統 IHC 的性能對比。
接下來,研究人員采用扁桃體組織驗證雙模式連續免疫熒光染色策略,通過多通道IF預篩選生物標志物后,經光漂白處理再進行全腔室六重免疫熒光染色(圖4)。對三個重復樣本的分析顯示,細胞表型組成高度相似,t-SNE聚類能清晰區分免疫細胞譜系。驗證了Dumi在復雜流程中的穩定性和數據可靠性。
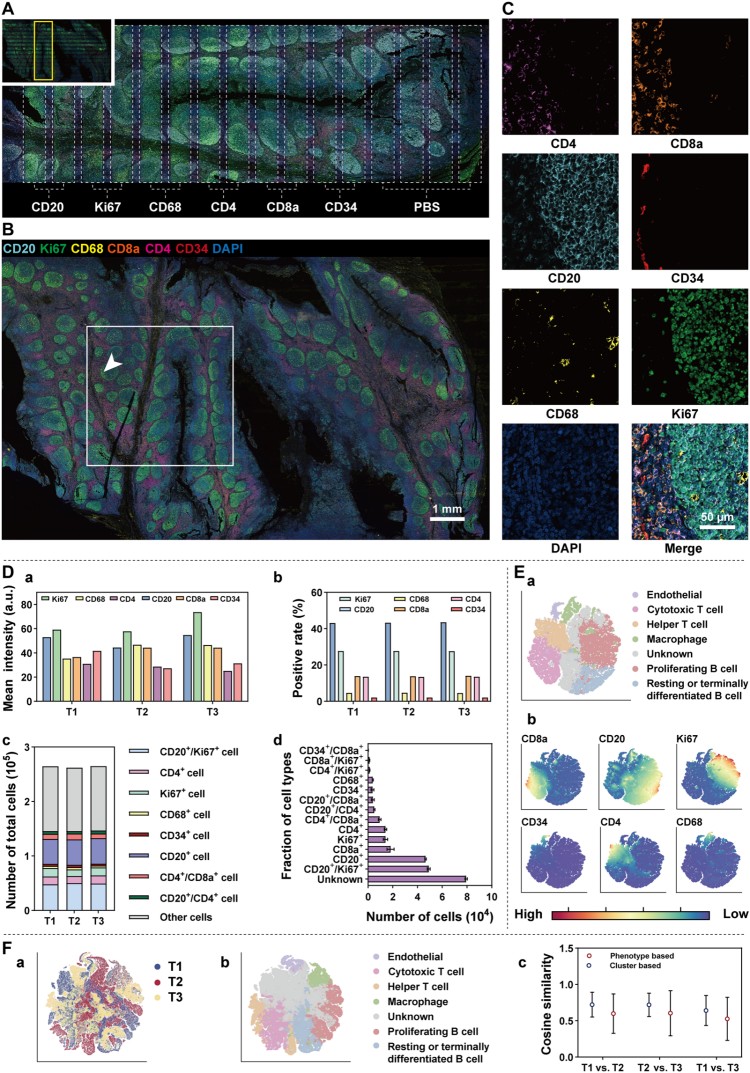
圖4. 雙模式連續染色的重復性與細胞分析。
在臨床應用中,研究團隊將Dumi用于4例彌漫大B細胞淋巴瘤(DLBCL),含1例罕見的原發于中樞神經系統彌漫大B細胞淋巴瘤(PCNS-DLBCL)。病理診斷結果顯示,通過多通道模式快速完成了自動化的16種生物標志物檢測,并請病理學家進行診斷,亞型診斷結果與病理報告高度一致。
基于PCNS-DLBCL樣本診斷后的剩余單切片,通過全腔室模式構建六重TME圖譜,涵蓋腫瘤細胞、免疫細胞、血管內皮細胞等。PhenoGraph聚類成功識別出細胞毒性T細胞、輔助 T細胞等群體。空間分析顯示,CD8a?T細胞與腫瘤細胞(CD20?)呈空間排斥關系,Ripley's K分析證實其在10 μm以上存在持續聚類,揭示了“免疫排斥型”TME特征,為TME研究提供了可重復的分析起點。
最后,研究人員在單一組織切片上實現多通道診斷標志物與全腔室TME圖譜的聯合分析。NND分析顯示,CD20?細胞與GFAP?細胞、CD68?細胞空間距離最近(中位距離8-10 μm)。不同診斷標志物陽性細胞的微環境存在差異:如MUM1?、Bcl-2?細胞與血管內皮細胞富集,c-Myc?細胞則呈排斥;Bcl-6?/CD20?、c-Myc?/CD20?細胞周圍的CD8a? T細胞比例升高,表明特定腫瘤亞群能主動塑造其微環境生態位,為個性化診療提供了直觀的空間證據。
總結:Dumi裝置借助摩方精密微納3D打印技術實現核心部件的高精度制備,突破性解決了罕見腫瘤樣本稀缺造成信息獲取不足的技術痛點。其雙模式設計可通過1-2張切片完成16種標志物診斷與TME空間分析,不僅大幅降低樣本消耗,節省了利用樣本進行單標記預實驗的篩選流程,還建立了診斷生物標志物與原位微環境的直接關聯,為解析腫瘤免疫逃逸機制提供了全新方法。該設備兼容現有臨床病理流程,無需復雜操作培訓,為罕見腫瘤的精準診斷、預后評估和個性化治療提供了實用工具,未來有望拓展至原位雜交、空間轉錄組等更多生物醫學應用場景。
原文鏈接:https://doi.org/10.1126/sciadv.aea2586











